O papel da proteína P2X7 na retinose pigmentar autossômica recessiva
A Revista Eletrônica PesquisABC possui o seguinte registro ISSN: 2675-1461
Gabriela Maria Badin a, Theo Henrique de Lima Vasconcellos b, Juliane Midori Ikebara c , Alexandre Hiroaki Kihara d
a Discente do curso de graduação “Bacharelado em Ciência e Tecnologia (BC&T)” da Universidade Federal do ABC (UFABC)
b Discente do programa “Pós-graduação em Biossistemas” da Universidade Federal do ABC
c Pesquisadora colaboradora da Universidade Federal do ABC
d Docente da Universidade Federal do ABC
Resumo: A retina é um tecido fotossensível presente na região interna do olho, responsável pela conversão da informação luminosa em informação eletroquímica, processo que tem início nos fotorreceptores. Quaisquer alterações nessas células podem levar a déficits visuais, dentre esses a retinose pigmentar (RP), essa patologia possui milhares de novos casos anuais contudo não tem cura e carece de tratamentos eficientes. Essa retinopatia leva a perda irreversível da visão, iniciando com a morte dos fotorreceptores do tipo bastonetes e posterior degradação dos cones e conta com diversos eventos, como o estresse oxidativo e a resposta inflamatória exacerbada. Parte dessa resposta é modulada pelo ATP e receptores purinérgicos, como o receptor P2X7, presente em diversas células da retina e que atua na neuroinflamação ativando células gliais. Os resultados indicam que a proteína P2X7 tem um papel relevante no decorrer da maturação da retina no animal saudável e no desenvolvimento da patologia no animal de RP autossômica recessiva. Através do bloqueio farmacológico de P2X7 utilizando o fármaco brilliant blue G via injeção sub-retiniana no modelo rd1, observa-se uma tendência neuroprotetora, com a redução da gliose reativa nos grupos tratados, demonstrado pelo marcador glial GFAP, também demonstra uma modulação da expressão da proteína rodopsina, presente nos bastonetes.
Palavras-chave: retina; retinose pigmentar; neuroinflamação; gliose reativa
Abstract: The retina is a crucial central nervous system (CNS) component. It converts light signals into electrochemical information, a process initiated by photoreceptors. An imbalance in the retina's physiological conditions or changes in functional photoreceptor numbers can lead to significant vision loss. A prominent example of vision loss is retinitis pigmentosa (RP). There are thousands of new cases of this pathology every year, but there is no cure and there are no effective treatments. This retinopathy starts with the death of rod photoreceptors and the subsequent degradation of cones involving events such as oxidative stress and an exacerbated inflammatory response. Part of this response is modulated by ATP and purinergic receptors, such as the P2X7 receptor. P2X7 is present in several retinal cells and acts in neuroinflammation by activating glial cells. The results indicate that the P2X7 protein plays an important role in the maturation of the retina in healthy animals and in the development of the pathology in the autosomal recessive RP animals. The pharmacological blockage of P2X7 with brilliant blue G via subretinal injection in the rd1 model, showed a neuroprotective tendency, reducing the reactive gliosis in the treated groups, as demonstrated by the glial marker GFAP, also showing a modulation of the expression of the protein rhodopsin, present in rods.
Keywords: retina; retinitis pigmentosa; neuroinflammation; P2X7; reactive gliosis
Este endereço de email está sendo protegido de spambots. Você precisa do JavaScript ativado para vê-lo.
ORCID ID: 0009-0003-2334-4869
Introdução
Como a retina funciona?
A retina é um tecido altamente especializado, cuja função principal é a visão, um dos sentidos mais importantes para a comunicação e interação do ser humano com o mundo. Ela é formada por várias camadas, compostas por diferentes tipos de células especializadas, conforme ilustrado na Figura 1. A primeira camada é composta pelos fotorreceptores, localizados na camada nuclear externa (outer nuclear layer, ONL), responsáveis pela fototransdução, processo de conversão da luz em sinais eletroquímicos que podem ser interpretados pelo cérebro. Existem dois subtipos de fotorreceptores: os cones e os bastonetes. Os cones são responsáveis pela percepção de cores e apresentam sensibilidade específica às cores verde, vermelho e azul. Já os bastonetes são fundamentais para a visão em condições de baixa luminosidade (visão noturna). Os fotorreceptores são células bastante únicas, compostos por terminal sináptico, núcleo, segmento interno e externo. A passagem de informação dos fotorreceptores se dá por meio de uma série de eventos intracelulares que convertem a absorção de luz em uma resposta fisiológica (1).
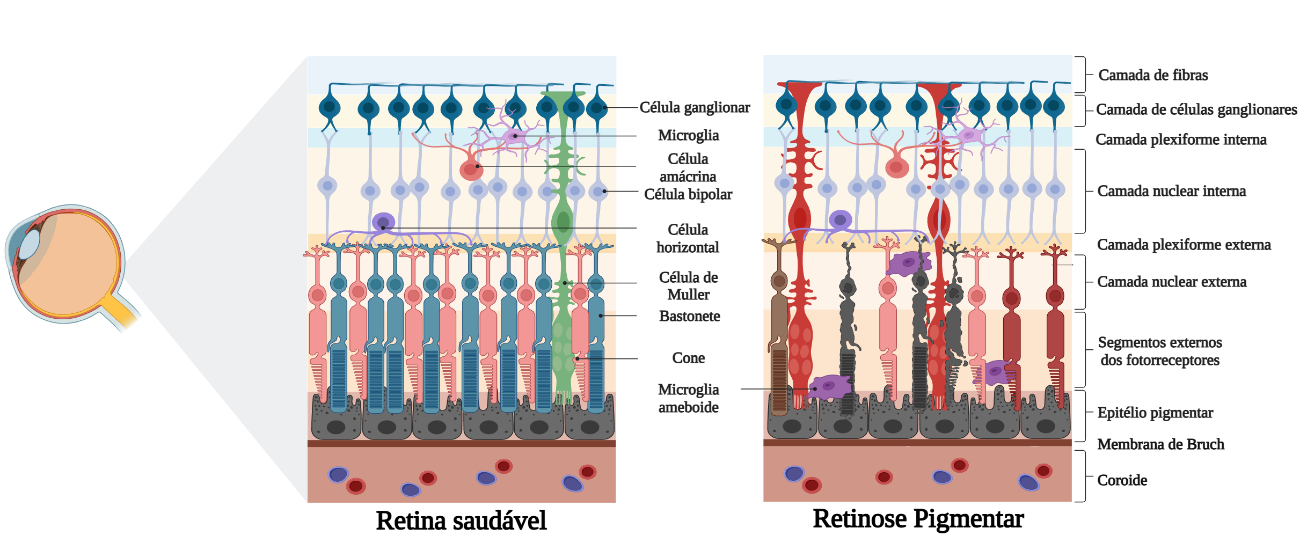
Figura 1. Ilustração esquemática da retina saudável e da retina na retinose pigmentar. Criado em BioRender.com
A informação é transmitida pelos fotorreceptores por meio do neurotransmissor glutamato, uma molécula sinalizadora, para as células horizontais e células bipolares presentes na camada nuclear interna. Em seguida, o sinal é transmitido em direção às células ganglionares da retina, que possuem axônios longos que formam o nervo óptico, que levará a informação visual até o cérebro. Outras células muito importantes da retina são as células gliais. A célula de Müller é o tipo de célula glial mais presente na retina, além dela, podemos encontrar astrócitos e microglia, que desempenham funções essenciais para o bom funcionamento da retina (1).
Próximo aos fotorreceptores, está disposto o epitélio pigmentar, que ajuda no bom funcionamento dessas células, é reconhecido por sua coloração escura, devido à produção de melanina. Esse epitélio pigmentar apresenta alta atividade metabólica, disponibilizando e reciclando moléculas necessárias para o ciclo da visão (1, 2). Devido a todas essas células complexas, a retina é como uma máquina bastante sensível que precisa de um ambiente bem específico para funcionar de forma adequada. Qualquer problema nessa máquina pode causar doenças nos olhos, as chamadas distrofias retinianas, como retinopatia diabética, glaucoma, degeneração macular relacionada à idade e retinose pigmentar. Essas doenças podem levar à perda completa da visão
A Retinose pigmentar e o receptor P2X7
A retinose pigmentar (RP) é considerada a maior causa de cegueira do mundo, sendo uma doença genética. Atualmente, estima-se que um a cada 3000 a 8000 indivíduos seja afetado pela doença (3,4). De modo geral, a RP apresenta três estágios: o estágio inicial, intermediário e tardio (3,5,6). O estágio inicial acontece entre as primeiras duas décadas de vida, com sintomas como dificuldade em enxergar à noite e uma redução da visão periférica ou visão em túnel, porém na luz do dia estes sintomas se tornam menos evidentes e mais difíceis de serem diagnosticados — conforme a idade avança a doença evolui progressivamente para cegueira (3,5,6).
Embora essa doença seja amplamente estudada, e seus sintomas bastante conhecidos, ainda não sabemos exatamente o que leva os fotorreceptores a morrerem— além disso, não há cura ou tratamento efetivo para os pacientes de RP, tornando essa doença um problema de saúde pública. Sabemos que alguns processos estão associados ao avanço da doença, como o desenvolvimento de uma forte resposta inflamatória, parecida com o que acontece quando cortamos o dedo, onde o tecido fica sensível e avermelhado, mas na RP é a morte dos fotorreceptores que leva as células da glia, microglias e células de Müller a promover a inflamação (7). Em parte, essa resposta ocorre pela percepção/captação de ATP, por um tipo de receptor presentes nessas células, os receptores P2X7, que desencadeiam resposta inflamatória diante da morte celular de neurônios (8,9).
A proteína P2X7 é uma proteína presente na membrana de algumas células. Imagine essa proteína como um sensor de incêndio muito sensível, mas nesse caso, em vez de fumaça o que ele detecta é uma pequena molécula, o ATP, que costuma ser um sinal de dano celular no tecido. Esse sensor está presente em células gliais e alguns neurônios, está envolvido nos processos inflamatórios e na liberação de citocinas, que são moléculas sinais relevantes em respostas inflamatórias (10,11). Ainda, esse receptor também atua de forma significativa em doenças neurodegenerativas, e em processos neuroinflamatórios como indicado na Figura 2 e neurogênicos (10).
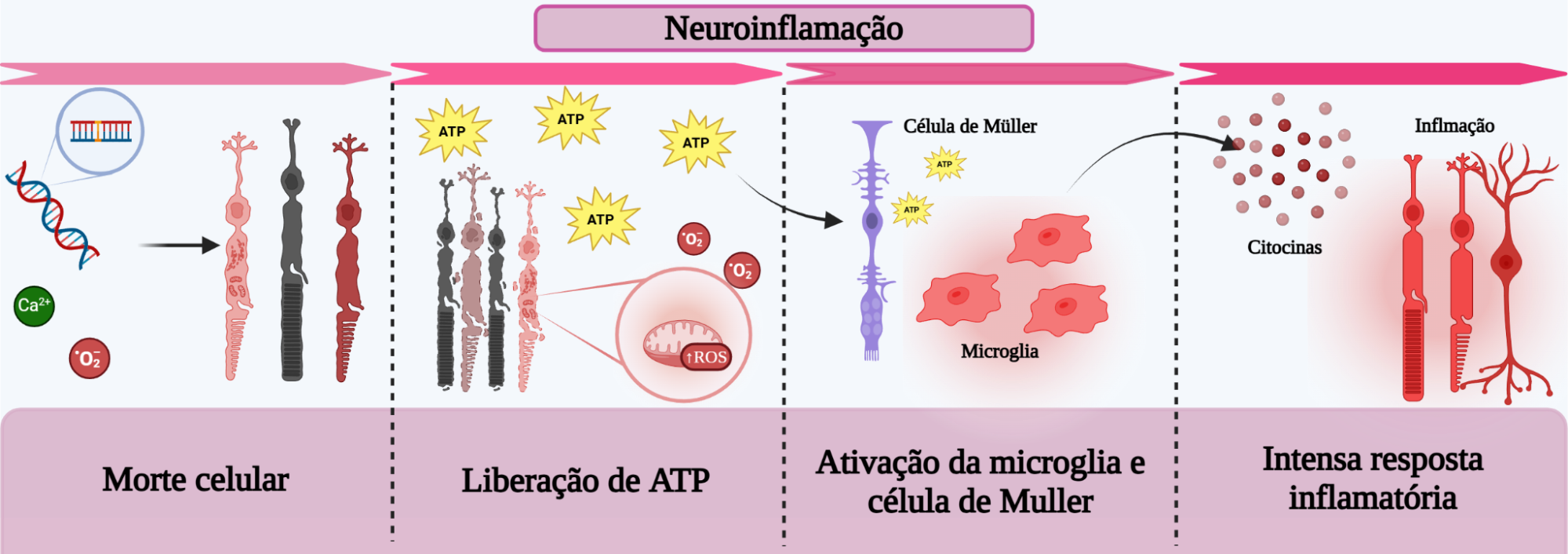
Figura 2. Processo de ativação dos processos neuroinflamatórios na retinose pigmentar. Criado em BioRender.com.
Por isso o objetivo deste trabalho, desenvolvido no Laboratório de Neurogenética da Universidade Federal do ABC, foi analisar o padrão de expressão e localização dos receptores P2X7, e as consequências do seu bloqueio farmacológico por brilliant blue G (BBG), durante o desenvolvimento da retina em camundongos saudáveis C57/BL6 (wt) e na progressão da RP em modelo de camundongo com retinose pigmentar C3H/HeJ (rd1), daqui para frente chamados de rd1.
Metodologia
Os camundongos foram provenientes do Instituto de Ciências Biológicas (ICB) da Universidade de São Paulo (USP) ou Criação da UFABC (Santo André), com idades de 7, 9, 14, e 21 dias pós-natal. Todos os procedimentos foram realizados de acordo com o aprovado no Comitê de Ética da Universidade Federal do ABC (CEUA #9432030818) (Figura 3).
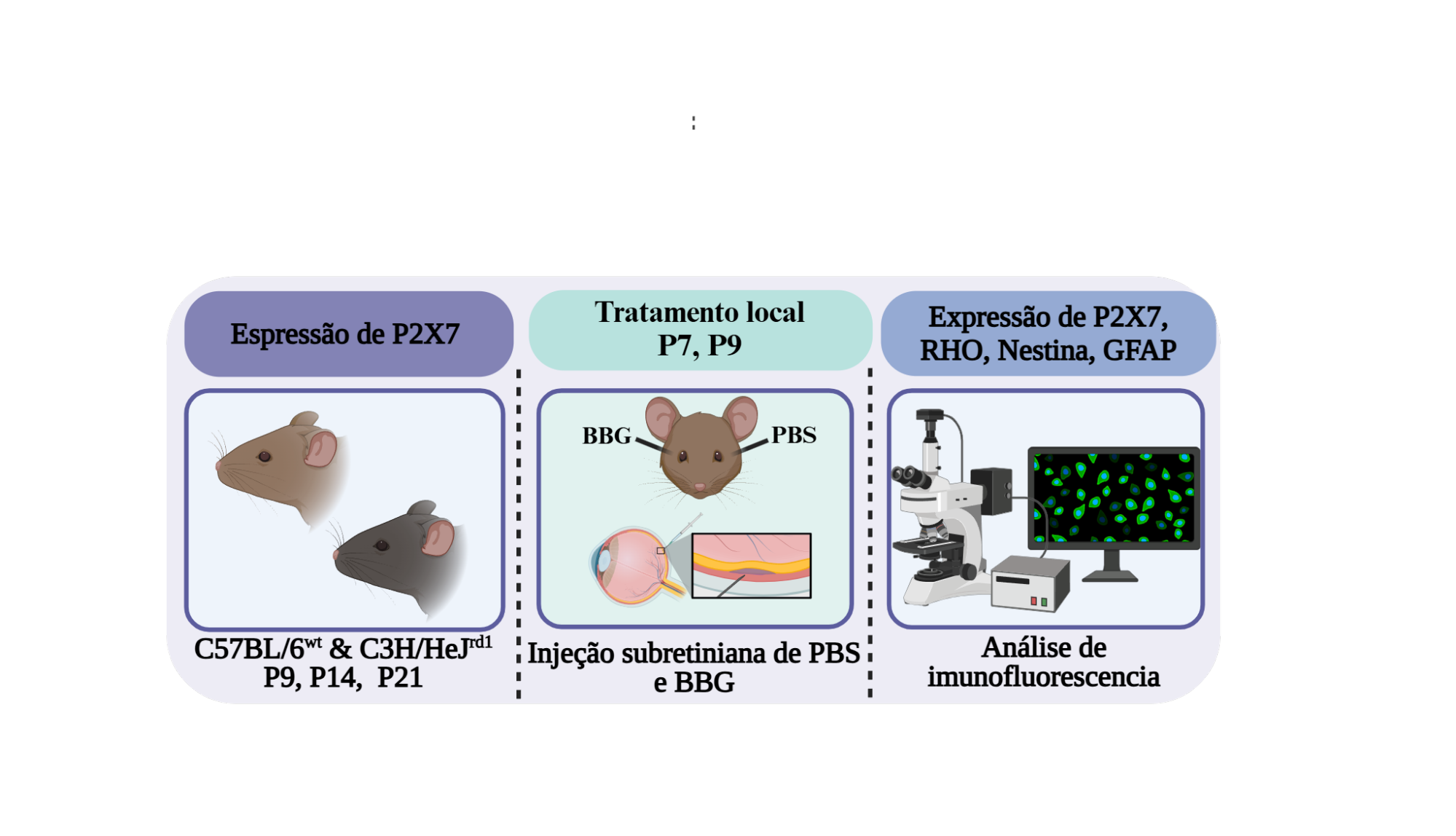
Figura 3. Metodologia aplicada. Criado com Biorender.com
Em nossa pesquisa, coletamos a retina de alguns animais tanto saudáveis (wt) quanto doentes (rd1) em diferentes fases da vida. Com outros animais, que apresentavam a retinose pigmentar (rd1), fizemos uma cirurgia bem simples. Nesse procedimento, colocamos um remédio que bloqueia a ação da P2X7 (BBG) em um dos olhos e um líquido sem remédio no outro (PBS), para comparar os resultados. Depois de um tempo, os animais foram examinados e seus olhos foram retirados para análise em um microscópio. Usamos técnicas específicas para marcar e identificar algumas proteínas das células da retina.
Resultados e discussão
Para entender a distribuição por localização do receptor P2X7 na RP autossômica recessiva, foi aplicada a técnica de Imunofluorescência (IF) em idades importantes do desenvolvimento da patologia. Observando os resultados, notamos que a principal diferença entre os grupos é que, na camada onde se localizam os fotorreceptores, há uma redução da intensidade de fluorescência no modelo doente, indicando que a proteína diminui nessa camada conforme o avanço da degeneração. Em contrapartida, outros estudos realizados com modelos de retinose pigmentar mostraram um aumento dessas proteínas coincidentes com o avanço da patologia. A análise de localização indicou que a proteína P2X7 está mais próxima ao núcleo conforme o avanço da RP, apresentando diferença já no início da vida. Interessante notar que, no animal wt não foram observadas diferenças durante o desenvolvimento.
Para observar os efeitos do bloqueio farmacológico com o brilliant blue G, foi necessário definir qual idade do desenvolvimento da RP ideal para realizar o bloqueio. Para isso, fizemos experimentos nos animais rd1 injetados no 7º e 9º dias de vida, coletados ambos com 14 dias. Contudo, ambos os ensaios não apresentaram diferenças estatísticas na área da camada dos fotorreceptores. Uma vez que não observamos diferenças estatísticas, decidimos analisar o estado da neuroinflamação nessas retinas, pois o receptor P2X7 está intimamente relacionado às células gliais da retina.
Ficou evidente pelos resultados que a proteína rodopsina, presente em bastonetes, estava menos presente nos olhos tratados com o remédio. Além disso, a imunofluorescência com marcador para GFAP (associado a astrócitos e células de Müller) mostrou uma redução no grupo tratado, indicando que o tratamento foi capaz de reduzir a resposta inflamatória. Ainda, para avaliar células de Müller e gliose reativa, utilizamos o marcador de nestina, mas não obtivemos redução significativa no grupo tratado.
Conclusão
Em resumo, os resultados deste trabalho sugerem que a P2X7 além de desempenhar um papel relevante na maturação da retina e na progressão da retinose pigmentar, seu bloqueio farmacológico levou a redução de uma importante resposta inflamatória, a gliose reativa. É possível concluir que, apesar de ter avançado em pontos essenciais, ainda é necessário explorar melhor, tanto o papel que a P2X7 desempenha na retina, de ambos os modelos, quanto os efeitos do bloqueio farmacológico na RP. Apesar de não ter resultados significativos na idade avaliada, ainda é possível que haja diferenças ao realizar o bloqueio em outras idades, bem como avaliar o efeito final em demais momentos da progressão da doença.
Além disso, é importante aprofundar os conhecimentos acerca da influência da P2X7 sobre a resposta de gliose reativa na RP, buscando compreender a influência da inibição do receptor P2X7 nas funções da microglia e células de Müller e em outros aspectos da neurodegeneração. Com isso, podemos obter informações valiosas sobre o papel do P2X7 na RP e abrir caminho para o desenvolvimento de novas terapias direcionadas para essa doença neurodegenerativa, que permanece sem cura e tratamentos efetivos.
Agradecimentos
Agradeço ao Programa de Iniciação Científica da UFABC, ao CNPq pelo apoio financeiro, à UFABC pela infraestrutura fornecida, e a minha equipe de laboratório que tornou essa pesquisa possível.
Referências Bibliográficas
- Hildebrand GD, Fielder AR. Anatomy and Physiology of the Retina. Pediatric Retina p. 39–65 (2011).
- Ali MU, Rahman MSU, Cao J, Yuan PX. Genetic characterization and disease mechanism of retinitis pigmentosa (2017).
- Hayes RP, Roderick TH. Prevalence of Retinitis Pigmentosa. Maine. J Ophthalmol (1984).
- Verbakel SK, van Huet RAC, Boon CJF, den Hollander AI, Collin RWJ, Klaver CCW, et al. Non-syndromic retinitis pigmentosa. Prog Retin Eye. (2018).
- Komeima K, Rogers BS, Lu L, Campochiaro PA. Antioxidants reduce cone cell death in a model of retinitis pigmentosa. Proc Natl Acad Sci (2006).
- Ronald C. Pruett M. Retinitis Pigmentosa: Clinical Observations and Correlations (1983).
- De Sousa, E. et al. VDAC1 regulates neuronal cell loss after retinal trauma injury by a mitochondria-independent pathway. Cell Death & Disease, v. 13, n. 4, p. 1–14. (2022).
- Vessey KA, Jobling AI, Greferath U, Fletcher EL. The role of the P2X7 receptor in the retina: Cell signalling and dysfunction. Adv Exp Med. (2012).
- Andrejew R, Oliveira-Giacomelli Á, Ribeiro DE, Glaser T, Arnaud-Sampaio VF, Lameu C, et al. The P2X7 Receptor: Central Hub of Brain Diseases. Front Mol Neurosci. (2020).
- Sluyter R. The P2X7 receptor. Adv Exp Med Biol. (2017).
- Seetal Chavda. P2X7 Receptor Modulation of Visual Responses in the Retina. Institute of Ophthalmology, University College London (2014).

Redes Sociais